Kiến thức Hóa lớp 11 - Sách Giáo Khoa
1. Thí nghiệm
Chuẩn bị ba cốc : cốc a đựng nước cất, cốc b đựng dung dịch saccarozơ (đường kính trắng tinh khiết), cốc c đựng dung dịch NaCl rồi lắp vào bộ dụng cụ như hình 1.1.
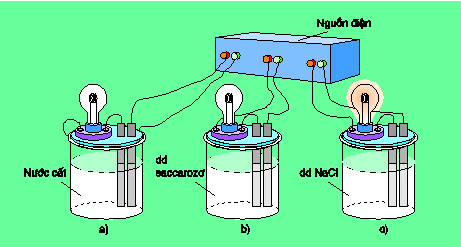
Hình 1.1. Bộ dụng cụ chứng minh tính dẫn điện của dung dịch.
Khi nối các đầu dây dẫn điện với nguồn điện, ta thấy chỉ bóng đèn ở cốc đựng dung dịch NaCl bật sáng. Vậy dung dịch NaCl dẫn điện, còn nước cất và dung dịch saccarozơ không dẫn điện.
Nếu làm các thí nghiệm tương tự, người ta thấy NaCl rắn, khan, NaOH rắn, khan, các dung dịch ancol etylic, glixerol không dẫn điện. Ngược lại các dung dịch axit, bazơ và muối đều dẫn điện.
2. Nguyên nhân tính dẫn điện của các dung dịch axit, bazơ và muối trong nước
Ngay từ năm 1887, A-rê-ni-ut đã chứng minh rằng, tính dẫn điện của các dung dịch axit, bazơ và muối là do trong dung dịch của chúng có các tiểu phân mang điện tích chuyển động tự do được gọi là các ion.
Như vậy các axit, bazơ và muối khi hoà tan trong nước điện li ra các ion, nên dung dịch của chúng dẫn điện.
Quá trình điện li các chất trong nước ra ion là sự điện li. Những chất tan trong nước điện li ra ion được gọi là những chất điện li.(*)
Vậy axit, bazơ và muối là những chất điện li.
(*) Nhiều chất khi nóng chảy cũng điện li ra ion, nên ở trạng thái nóng chảy các chất này dẫn điện được. Trong một số tài liệu, người ta cũng đề cập đến chất điện li loại này, thí dụ Al2O3.